Механизм восстановления окисных плен
Механизм восстановления окисных плен
В процессе вакуумирования металла из него удаляются не только растворенные кислород, водород и азот, по и неметаллические включения (табл. 1).
Плавка в вакууме прежде всего исключает возможность образования окислов и нитридов.
В условиях вакуума химическая реакция кислорода с углеродом и водородом или с другим растворенным в металле элементом, образующим летучие окислы, идет гораздо быстрее, чем в атмосфере воздуха, благодаря тому, что газообразные продукты реакции непрерывно удаляются. Особенно интенсивно идет раскисление металла в вакууме в присутствии углерода, который при низких остаточных давлениях газа над металлом является более энергичным раскислителем, чем кремний и алюминий.
Углерод при взаимодействии с кислородом, растворенным в жидком металле, образует нерастворимый окисел в газообразном состоянии. Константа равновесия
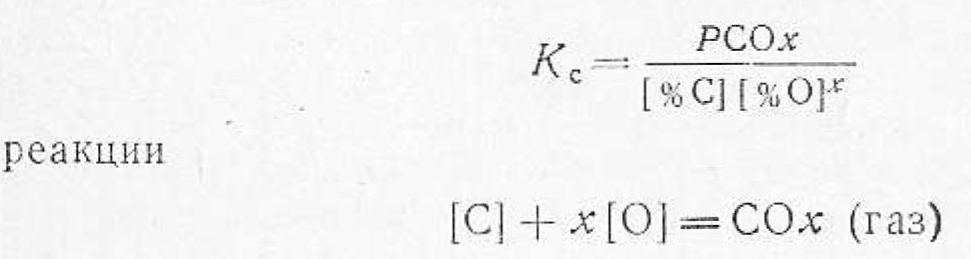
и данной температуре не зависит от давления образующейся "азовой фазы (главным образом окиси углерода). Однако снижение давления этой газообразной фазы при постоянном значении константы равновесия, естественно, сопровождается уменьшением значения произведения. Таким образом, применение вакуума является средством повышения раскислительпой способности углерода [12].
Следовательно, кроме удаления поглощенных сплавом газов.
вакуумная плавка создает условия для восстановления окислов.
Подробное изучение влияния плавки в вакууме па процесс восстановления окисных плен показывает, что этот метод является весьма эффективным для борьбы с окисными пленами.
Интенсивность восстановления окисных плен зависит от многих факторов: величины вакуума, температуры жидкого металла, количества находящегося в сплаве углерода и др. Наблюдение, за поверхностью жидкой ванны при плавке в вакуумной индукционной печи показывает следующее: при расплавлении металла окисные плены, находящиеся в слитках, всплывают на поверхность и сплошным слоем закрывают все зеркало металла. При нагреве и перемешивании металла слой окисных плен становится тоньше, количество плен уменьшается и остатки их распределяются в виде ободка по стенкам тигля. С увеличением температуры и времени выдержки металла под вакуумом количество плен продолжает уменьшаться. Особенно заметным становится восстановления плен возрастает также с повышением величины вакуума. При низком вакууме плены восстанавливаются в случае перегрева металла до высоких температур. При наличии же высокого вакуума таких перегревов пе требуется. Резюмируя сказанное, можно сделать следующий вывод: восстановление окисных плен происходит тем интенсивнее, чем выше температуря металла, чем больше выдержка жидкого металла под вакуумом, чем значительнее величина вакуума и чем больше углерода содержится в данном сплаве. Механизм восстановления окисных плен можно объяснить следующим образом.
исчезновение плены при повышении температуры металла до 1600—1650° и выдержке при этой температуре. Восстановление окисных плен происходит значительно интенсивнее (при тех же величинах вакуума, температурах нагрева и выдержках) в случае дополнительного введения в жидкий металл углерода. Происходит бурное кипение металла, сопровождающееся выделением пузырьков черного цвета. Зеркало металла быстро освобождается от плен. Наблюдения показывают, что если в вакууме переплавлять сплав, в котором совершенно отсутствует углерод, то восстановление окисных плен почти не наблюдается. Интенсивность
В состав некоторых литейных жаропрочных сплавов входят такие элементы, как никель, хром, алюминий, титан, молибден и др. Эти элементы при плавке и разливке сплава активно соединю! ся с кислородом воздуха с образованием окислов, наблюдаемых в виде пленки, плотно покрывающей все зеркало металла Рассматривая кривые зависимости свободной энергии образов^ шгя окислов от температуры, можно заключить, что при повыщ/ нии температуры тепловой эффект их уменьшается, стремления к реакции замедляются и устойчивость окисла уменьшается, а при определенной температуре идет диссоциация окислов с поглоц(е. нием тепла (фиг. 3).

Известно также, что сродство к кислороду у металлов с повышением температуры понижается. Для углерода, наоборот’, сродство к’ кислороду с повышением температуры повышается. ЭФо говорит о том, что борьбу с пленообразованием можно вести двумя путями: а) нагревом сплава при плавке до высоких температур и б) восстановлением окислов в зоне высоких температур углеродом.
Для проверки предположения о том, что именно наличие над перегретым металлом вакуума приводит к необратимому исчезновению плены, было проведено расплавление металла под вакуумом с последующим заполнением камеры аргоном. В результате проведения серии таких плавок было установлено, что при перегреве металла и выдержке его под аргоном плена временно исчезает, но потом вновь появляется при его остывании.
Таким образом, единственным объяснением необратимого исчезновения ее может служить наличие над расплавом пониженного давления,
Выше было сказано, что для углерода сродство к кислороду с увеличением температуры повышается.
Этим и объясняется возможность восстановления довольно прочных окислов металлов углеродом при высоких температурах. Как видно из фиг. 3, для восстановления, например, окиси алюминия нужна температура около 2000°. Но получить такие высокие температуры при обычных условиях сталеварения в атмосфере воздуха невозможно, поэтому в этих плавках и невозможно восстановить окислы углеродом. Вакуум, как известно, смещает реакцию 2СтРО2 = 2СО вправо. Это означает, что вакуум снижает начальную температуру восстановления окислов углеродом.
О возможностях снижения в вакууме начальной температуры восстановления окислов углеродом свидетельствуют данные, приведенные в табл. 2. Как видно из табл. 2, температура начала вос-4ПлИ0Вле?ия окислов металлов углеродом в вакууме снижается па 4U0—600". Это означает, что при выдержке металла при пониженном давлении реакции восстановления протекают при 1500—1600′, т. е. при температурах, вполне достижимых при работе на индукционных печах. 1 акпм образом, создаются условия для протекания реакции МеО-|-С=—Ме-гСО , сопровождающейся выделением пузырьков окиси углерода.
Следовательно, причиной необратимого процесса исчезновения плены является реакция восстановления ее углеродом, интенсивно протекающая в условиях пониженного давления и высокой температуры. Чем больше в сплаве углерода, тем интенсивнее протекает восстановление. При дополнительном введении свободного
Т а б лица 2
Температуры начала восстановления окислов углеродом в вакууме и при обычном давлении
|
Окисел |
Температура в °C |
|
|
в вакууме |
при давлении 760 мм рт. ст. |
|
|
Сг,О3 |
690 |
1105 |
|
TiO2 |
1100 |
1700 |
|
SiO2 |
1250 |
1560 |
|
MgO |
1350 |
1800 |
|
AI2O2 |
1350 |
1950 |
углерода в расплав в виде прутка графита или электродного боя восстановление плен происходит наиболее полно. И, наоборот, при полном отсутствии углерода в сплаве восстановление плен в вакууме не происходит. При этом обнаруживается, что если сплав, не содержащий углерода, окислить и затем подвергнуть вакуумированию, то плена полностью не исчезает, но характер ее по сравнению с первоначальной пленой становится иной. При вакуумировании и повышении температуры металла плена сначала исчезает, а перед кристаллизацией расплава появляется вновь, по уже в меньшем количестве, менее толстая и менее вязкая.
Изменение характера плены без ее полного исчезновения, по-видимому, обусловлено протеканием других реакций, кроме реакции образования окиси углерода, сопровождающихся образованиями летучих соединений.
По мнению некоторых исследователей, к реакциям образования летучих соединений можно отнести образование летучих соединений алюминия с кислородом при пониженной валентности алюминия.
Предположение о возможности соединения кислорода с алюминием пониженной валентности, т. е. о существовании так называемой «субокиси» (А12О), высказано в работе [1-1]. Существование низшего окисла алюминия в газообразном состоянии было установлено спектрометрическим [15] и масспектрометрическим методами при выдержке смеси порошков алюминия и окиси алюминия при высокой температуре в вакууме.
Из всего сказанного можно сделать следующие выводы: в механизме восстановления окисных плен в вакууме основной реакцией является реакция взаимодействия углерода, находящегося в металле, с кислородом окисных плен. Эта реакция сопровождается бурным кипением расплава с выделением газовых пузырей. Побочную роль играет реакция образования летучей суб-скиси алюминия.


