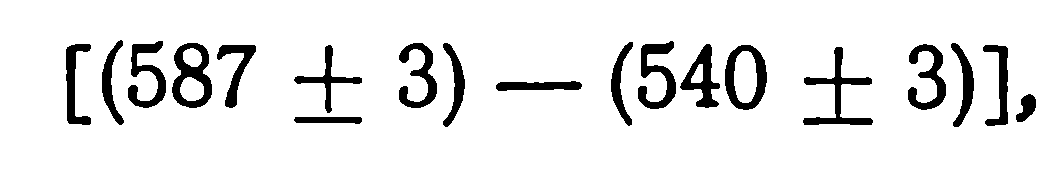Основные соображения при конструировании аналитической системы
Основной задачей при конструировании аналитической системы является правильный выбор размеров газоизмерительной бюретки (или манометра Мак-Леода) для определения количества газов (СО, N2 и Н2) в достаточно широких пределах и в то же время с высокой степенью точности.
На фиг. 4 показана газоизмерительная бюретка, применяемая в настоящее время. Она состоит из трех калиброванных объемов (Vi> Т2, К3), и может быть использована как газоизмерительная бюретка и как обычный манометр Мак-Леода. Если она используется как газоизмеритель, газ перегоняется в нее с помощью ртутного насоса Теплера. Собранный газ можно сжать в любом из трех тщательно калиброванных объемов путем поднимания ртути до меток В, С или D. По разности высот между уровнем ртути до измеряемой метки и уровнем ртути в параллельном капилляре измеряется давление газа. В табл. 1 приведены пределы количества газов, которые могут
Таблица 1
Емкость газовой бюретки
Для измерения больших количеств газа к измерительному объему добавляется объем расширительного баллончика А, что увеличивает емкость прибора приблизительно в 10 раз. Каждый из объемов бюретки откалиброван с точностью до долей процента. Если предположить, что оператор в состоянии произвести отсчет с точностью до 1 мм рт. ст., то погрешность измерений для каждого из объемов составит 0,35, 1,0 и 3,0 мл • мм соответственно. Измерение газа может производиться в любом из калиброванных объемов в зависимости от общего количества газа и желаемой степени точности.
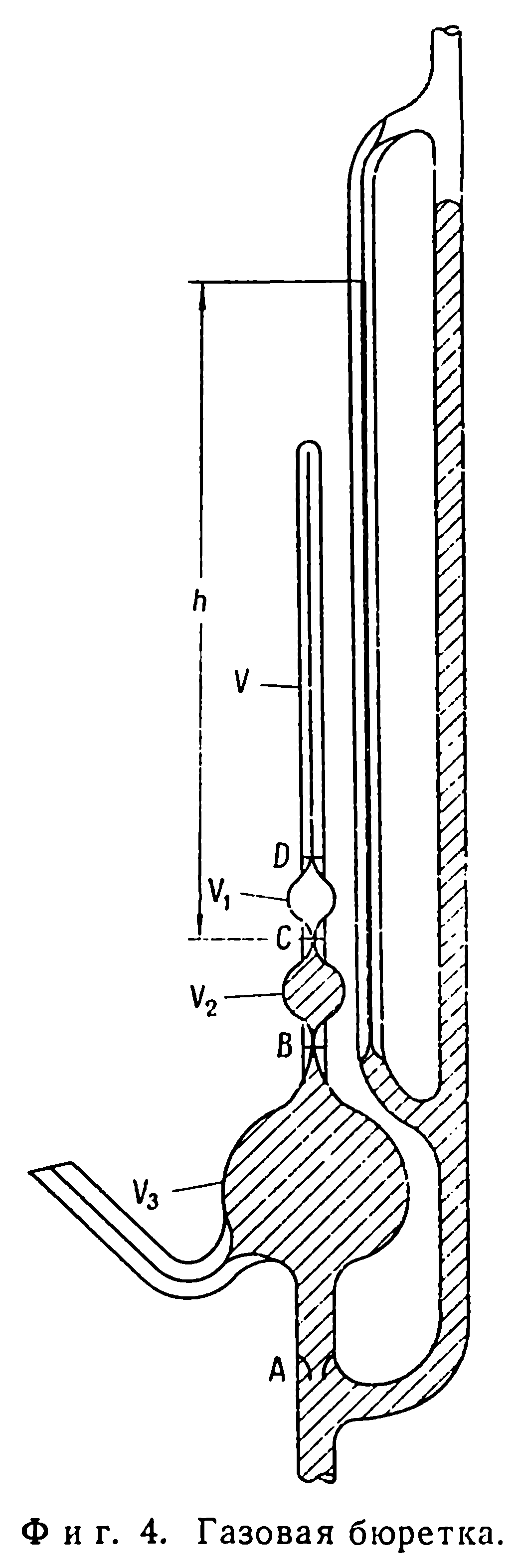

Так, например, при определении количества газа, равного которая при крайних значениях ошибки дает 47 + 6 мл • мм. В таких случаях точность анализа может быть повышена путем вымораживания СО2 с помощью жидкого азота и эвакуации азота из системы. Это дает возможность определить содержание СО2 также в наименьшем объеме бюретки (в первом калиброванном объеме), где точность измерения значительно выше. К сожалению, этот прием нельзя использовать при определении водорода, так как водяные пары во время анализа газов непрерывно удаляются. Вследствие этого результаты определения водорода могут несколько меняться в зависимости от его содержания по отношению к количеству остальных газов. Этот вопрос будет рассмотрен особо.
В заключение следует отметить, что при правильном проектировании и тщательной сборке установки пределы ошибок измерения не будут превышать 1% при содержании в пробе кислорода и азота 0,001% или выше. При очень малом содержании газов степень точности анализа, очевидно, будет низкой. Предположим, что содержание кислорода в пробе 4 г металла составляет 0,0001%. Это количество кислорода при реакции с углеродом даст всего лишь 5 мл • мм окиси углерода. При измерении газа в первом калиброванном объеме бюретки пределы погрешности не должны превышать +0,35 мл • мм или 7% от определяемой величины (табл. 1). В действительности же погрешность анализа может быть увеличена за счет нормального газовыделения печи. Это количество газов может быть таким же, как и газов, выделяющихся из пробы (с 0,0001 % О2), поэтому погрешность измерения может возрасти до +20%.
Операции измерения выделенных газов можно выполнить, однако, с достаточно высокой степенью точности, поэтому они не могут служить заметным источником ошибок, присущих методу анализа газов вакуум-плавкой. Навеска анализируемой пробы металла зависит от емкости тазоизмерительной системы. В табл. 2 приведены количества водорода, •окиси углерода и азота (в мл • мм) при различных навесках металла и концентрациях газов. Пользуясь данными табл. 1 и 2, можно подобрать оптимальную пробу для различных аналитических случаев. Например, для анализа титана обычно используется проба весом 0,25 г. Обычный титановый сплав содержит около 0,1% кислорода, 0,0001% водорода и незначительное количество азота. Сумма количеств окиси углерода и водорода равна 535 мл • мм эту величину легко измерить в газоизмери-•гельной бюретке.
100 мл мм, погрешность измерения в первом калиброванном объеме (капилляре) составит +0,35, а во втором +1,0 мл • мм. Точно так же для перехода от второго к третьему объему при измерении количества газа в 300 мл • мм погрешность определения составит +1,0 и +3,0 мл • мм соответственно.
Таким образом, можно считать, что измерение количества собранного газа может быть выполнено с точностью до 1%.
Обычно количество СО2 определяется по разности между измерениями количеств азота и суммы азота с двуокисью углерода. Если измеряются значительные количества азота и небольшие—кислорода, то точность определения СО2 снижается, так как в каждое из двух измерений, по разности которых устанавливается количество СО2, вносится одна и та же величина абсолютной ошибки. Это можно видеть из данных табл. 2, в которой приведены значения количеств газов при различных содержаниях водорода, кислорода и азота. Так, например, если анализируется проба в 4 г металла, содержащая 0,001% кислорода и 0,02% азота, что в единицах pV составляет 47 и 540 мл • мм соответственно, то количество СО2 определяется из разности